세계 각국은 지금 지구온난화 위기에 따른 탄소중립을 실천하기 위해 노력하고 있다. 특히 온난화의 주범인 화석연료를 대체하기 위한 방안으로 수소와 암모니아에 대한 관심이 고조되고 있다. 이에 필자는 △왜 암모니아인가 △액화 암모니아의 특성 △암모니아 연료 CI엔진 등에 대해 3회에 걸쳐 연재한다.
암모니아 누설로는 불 안 붙어
동(銅) 등 각종 소재 부식에 경계해야

1. 액화 암모니아의 물리적 성질
액화 암모니아는 상온에서 무색의 심한 악취를 풍기는 물질로 인체에 위험성이 많은 가연성가스로 분류되고 있으나 순수 암모니아 가스 누설로는 불이 잘 붙지 않는다. 그러나 천연가스나 수소 등을 일정량 혼합시켜서는 대기오염 물질을 발생시키지 않는 청정연료로 활용이 가능하다. 한국과 일본 등에서는 가연성가스로 분류하고 있으나 미국 소방법에는 불연성가스로 분류하고 있다.
암모니아는 표준 상태에서 특유의 자극적 냄새가 나는 무색의 기체다. 밀도는 0.771g/ℓ(리터당 그램)이며, 이는 공기의 0.5971배에 해당한다. 상온에서도 압축시키면 비교적 간단하게 액화시킬 수 있다. 쌍극자 모멘트는 1.48D이다. 녹는점은 -77.7°C, 끓는점은 -33.4°C, 임계온도는 132.5°C이고, 임계압력은 112.5atm이다. 생성열은 11.042Kcal/mol, 융해열은 1.351Kcal/mol, 기화열은 5.58Kcal/mol이다. 액화 암모니아의 주요 요소별 기준치를 요약 정리된 물리적 특성을 아래 <표1>로 정리했다.
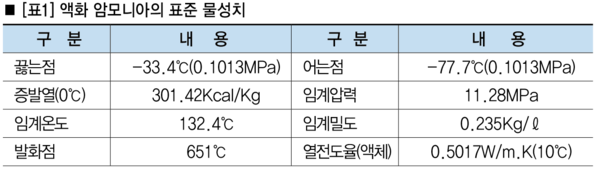
암모니아의 물리적 성질은 부분적으로 수소 결합에 영향을 받는다. <표2>는 암모니아의 온도별 증기압을 나타낸다.
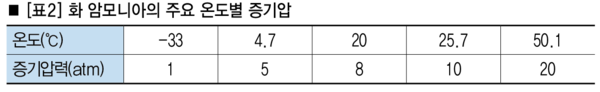
2. 액화 암모니아의 특성치
① 비중 : 가스 비중은 0.5962(25℃. 공기=1.)이다.
액체 비중은-0.6828Kg/ℓ(-33.7℃)이다.
② 밀도(Density) : 0.7708g/ℓ(표준상태. 실측치)
암모니아 밀도를 이상기체 상태 방정식으로 구하면은 분자량(g)/22.4(ℓ)=0.760g/ℓ이 된다. 따라서 실체 측정치와 이상기체 상태에서는 다소의 차 이가 있다.
③ 비체적은 1.297ℓ/g이다.
(1) 액화 암모니아의 상변화
액화 상태의 암모니아도 온도변화에 따라 물질의 상태가 변화한다. 물질의 상을 바꾸는 한 가지 방법은 열(에너지)을 더하거나 빼는 것이다. 예를 들어 물(액체)을 가열하면 수증기(기체)가 되고, 냉각시키면 얼음(고체)이 된다. 대부분 물질은 고온에서는 기체가 되고, 저온에서는 고체가 된다. 그리고 그 중간 온도에서 액체 상태를 취한다. 이와 같이 물질의 상태가 바뀌는 것을 상전이 또는 상변화라 부른다. 액체 암모니아의 상전이가 일어나면 물리적 성질도 변화가 일어난다. 예를 들어 액체를 계속 가열하면 어떤 온도에서 더 이상 온도가 증가하지 않고 갑자기 부피가 크게 증가하게 된다.
(2) 암모니아의 물에 대한 용해도
암모니아는 물에 잘 녹는 물질로 용액의 융점(어는점)에서 암모니아는 질량 퍼센트로 약 45퍼센트까지 녹을 수 있으며 표준 상태에서 암모니아는 질량 퍼센트로 약 30퍼센트까지 녹을 수 있다. 용해도는 0°C의 물에 89.9g/100mℓ(100밀리리터당 그램), 20°C의 물에 52.0g/100mℓ, 96°C의 물에 7.4g/100mℓ이며 20°C의 에탄올에서의 용해도는 14.8g/100mℓ이며 에테르에도 녹는다.
암모니아의 물에 대한 용해는 고온보다는 저온 시 용해도가 높다. 예를 들면 0℃ 때에는 1,176배 용해도를 가지며, 20℃일 때는 702배의 용해도를 갖는다. <표3>에 주요온도와 압력에 대한 용해도를 제시한다.
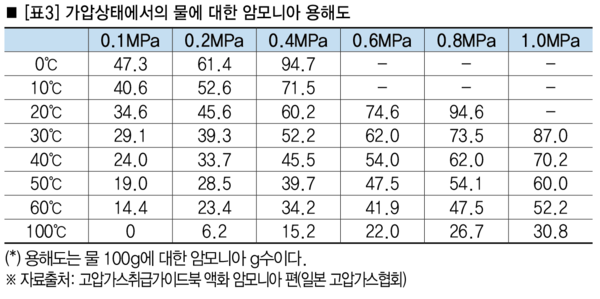
3. 액화 암모니아의 증기압 및 밀도
액화 암모니아는 상온 가압상태에서 쉽게 가스화 되어 수증기 상의 백연(白煙)상태로 변하며 공기보다 가벼워 쉽게 확산하여 증발한다. 암모니아는 액화온도가 섭씨 -33도에 불과하여 수소에 비해 액화처리 하는데 있어, 기술적 장벽이 없는 데다가 암모니아는 수소분자를 1.5개 포함하고 있어, 액화 수소 대비 단위 부피당 1.5~2배의 저장용량으로 대용량 저장이 가능하다는 장점이 있는 것으로 알려져 있다.
(1) 액화 암모니아 기화 시 가스의 비체적
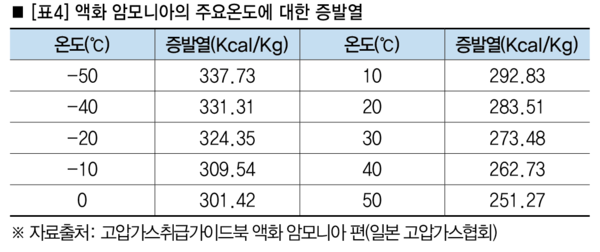
<표4>에 따라 액화가스 온도가 0℃, 이때 압력이 0.4232MPa이면 가스의 밀도 는 0.6341Kg/ℓ이 되며, 0℃, 1기압일 경우에는 1.297ℓ/g이 된다.
이를 정리하면 0℃, 1기압에서 액화 암모니아 1ℓ가 기화하면서 갖는 체적은
1ℓ x 0.6341Kg/ℓ x (1.297 x 1000ℓ/Kg)=822.4ℓ ≒ 800ℓ가 된다.
따라서 약 800배의 체적을 갖는다.
(2) 증발열
액체인 물질이 증발할 때 외부로부터 흡수하는 열을 의미한다. 증발열이 크면 증발할 때 주변의 열을 더 많이 흡수한다. 액체 상태인 분자들은 기체 상태보다 결합이 많이 되어 있는데 이 결합을 끊기 위해 열을 흡수하는 것이다.
이와 반대로 기체인 물질이 액체로 될 때는 같은 양의 열을 방출한다. 증발열의 예로는 여름에 물을 뿌리면 시원함을 느끼는 것 등이 있다.
4. 암모니아의 화학적 특성
암모니아는 비교적 안정적인 물질이지만 고압가스안전관리 법에는 가연성가스 및 독성물질로 규정하고 있어 취급에 많은 주의가 필요하다. 대표적인 화학적 반응을 황산과 염소와의 반응이다.
(1) 반응성
가) 황산과의 반응
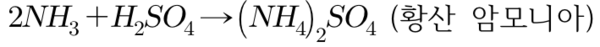
나) 염소와의 반응:
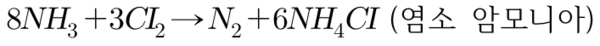
염소의 과잉반응으로 인해 생성된 암모니아가 염소와 반응하여 NCI₃가 생성한다.
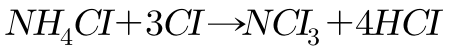
이 NCI₃이 유분 상태에서는 이상적으로 강한 폭발성 물질의 성분이 생성되 며, 암모니아 가스 누설을 검지하기 위하여 염산과 NH₄CI를 반응시켜 백 연(白煙)을 발생하게 한다.
다) 산화 환원반응
암모니아에 포함된 질소의 산화 상태가 바뀌는 반응과 수소가 해리(解離)되는 반응으로 나눌 수 있다. 전자의 예로는 다음과 같이 백금 촉매의 존재 하에 암모니아가 일산화질소(NO)로 산화되는 반응을 들 수 있다.
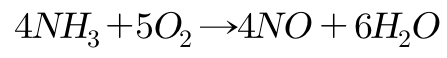
촉매가 존재하지 않는다면 암모니아는 산소로 인하여 연소되어 질소와 물을 만든다. 이 과정에서 소량의 질소암모늄, 이산화질소 등이 생성되기도 한다.
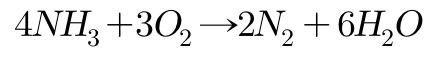
암모니아는 할로젠과 반응하여 산화되어 질소를 내놓고, 생성된 할로젠화 수소는 다시 암모니아와 결합하여 염을 만든다. 암모니아가 염소로 산화될 경우의 반응식은 다음과 같다.
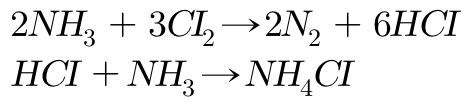
앞의 반응에서 염소가 과잉으로 있다면 다음과 같은 반응이 추가적으로 진 행되어 폭발성의 황색 기름인 삼 염화 질소가 생성된다.
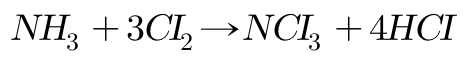
암모니아와 금속 산화물의 반응 역시 질소가 산화되는 반응이다. 다음은 암 모니아가 산 구리(II)와 반응하는 경우이다.
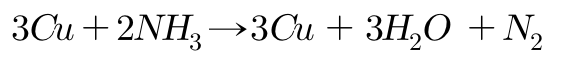
수소가 해리되는 반응의 예로는 금속과 암모니아의 반응을 들 수 있다.
반응성이 높은 금속과 암모니아가 반응하면 아마이드가 형성된다. 예를 들 어, 암모니아와 나트륨이 반응하면 나트륨아마이드가 생성된다.
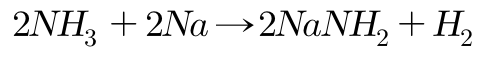
암모니아가 고온에서 마그네슘과 반응하는 경우 마그네슘이 암모니아의 모 든 수소 원자를 치환하여 삼차 아마이드인 질화마그네슘을 만든다. 반응식 은 다음과 같다.
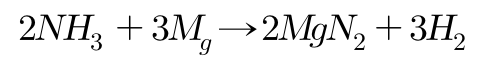
라) 암모니아의 열분해
암모니아는 고온에서 분해하여 수소와 질소를 생성한다.
마) 물과의 반응
물과는 이상적으로 잘 반응하여 약한 알칼리성을 띤 수용액을 생성한다.
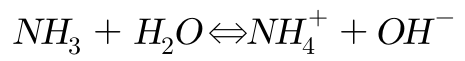
(2) 금속과의 작용
암모니아와 금속이온과의 결합은 착이온(complex ion)을 생성시키며, 산화물의 반응 역시 질소가 산화되는 반응이다. 수소가 해리되는 반응의 예로는 금속과 암모니아의 반응을 들 수 있다. 예를 들면 유산동의 수용액에 암모니아를 가하면 염기성 유산동(Cu(OH)₂.CuSO₄)의 청백색 침전이 생긴다.
이는 암모니아 누설검지용으로 활용이 가능하며, 여기에 암모니아수를 첨가시켜 염기성 유산동의 침전을 용해시켜 심청색의 동 암모니아 착염의 용액을 만들 수 있다. 이 성질은 암모니아를 사용하는 설비와 계측기에 동 및 동합금과 알루미늄, 알루미늄합금 사용을 방해하는 요인이 된다. 따라서 암모니아에는 통상 철과 스테인리스 강이 사용되고 있다. 암모니아는 독성과 부식성을 유발하는 화학물질로 활용 시스템의 재료선정에 전문적인 기술이 필요하다.
암모니아는 특히 동 및 동합금과 알루미늄합금 소재에 대한 부식에 특별히 경계해야 하는데, 구리―네이벌 황동(Naval brass) 및 알루미늄 황동을 포함한 아연 합금은 구리 합금 암모니아에 의한 응력 부식 균열 (NH₃SCC)에 가장 취약하다. 구리 합금 열교환기 튜브에서 암모니아 응력 부식 균열은 표면 균열, 녹색·연청 Cu-암모니아 부식 복합체(화합물) 및 튜브 표면에 단일 또는 고분 지형 균열을 형성하는 특징이 있다.
환경과 스트레스 수준에 따라 다르지만 액체 암모니아 응력 부식은 매체가 액체 암모니아의 작동 온도가 -5℃보다(물 함량 0.2% 이하) 공기(산소 또는 이산화탄소)에 의해 오염될 가능성이 있는 경우에 형성된다.
사례: 탄소강의 부식
탄소강은 간혹 3~4개월 만에 깊고 얕은 구덩이의 공식(pit)현상이 발생되기도 한다. 아래 그림은 탄소강에 발생한 암모니아 응력부식현상(현미경 관찰)을 나타낸다.

시간 경과에 따른 균열 성장 속도의 감소는 주로 균열 외부의 틈새 부식 공격에 의해 발생한다. 암모니아에서 탄소강의 SCC(Stress Corrosion Cracking)는 음극 분극에 의해 방지된다. 양극 분극이 높으면 SCC는 2,000ppm 물이 있는 암모니아와 산소가 없는 암모니아에서 발생한다.

